
Il trapianto cardiaco rappresenta la terapia più efficace nel trattamento dei pazienti affetti da scompenso cardia-co avanzato.Christian Barnard, chirurgo sudafricano, è stato il pioniere dei trapianti cardiaci.Barnard si era spe-cializzato in chirurgia cardiotoracica negli Stati Uniti d'A-merica.

Tornato in Sud Africa, creò la prima unità coronarica dell' ospedale Groote Schuur di Città del
Capo e dopo aver eseguito numerosi esperimenti sul cane, eseguì con suc-cesso la prima operazione a cuore aperto sull'uomo; era il 2 dicembre
1967.

Il paziente Louis Washkansky, al quale fu effettuato il pri-mo trapianto cardiaco era affetto da una grave forma di scompenso cardiaco; ricevette il cuore da una giovane donna di 25 anni, che in seguito ad un incidente era con-dannata ad una morte imminente. Quando l'operazione fu conclusa, Barnard si fermò a guardare per poi fare un passo indietro ed esclamare: «Funziona!».
L'entusiasmo che generò la notizia del primo trapianto cardiaco durò solo pochi giorni, con precisione 18 giorni, perchè Louis Washkansky non superò una polmonite bi-laterale che lo portò alla morte.Ciononostante Barnard non si perse d'animo e il mese successivo ritentò l'ope-razione sul dentista Philip Blaiberg di 58 anni che rice-vette l'organo dal giovane Clive Haupt di 24 anni, dece-duto per una emorragia cerebrale. Anche se il decorso fu piuttosto burrascoso, per le ripetute reazioni di rigetto, il paziente sopravvisse per più di 1 anno e mezzo. Il rigetto era dunque un ostacolo alla prolungamento della soprav-vivenza. Già il chirurgo Norman Shumway della Stanford University, nell'esperimento di trapianto nei cani, si era reso conto che il rigetto era una sorta di rifiuto immuni-tario ad accettare un corpo estraneo, e che in sintesi era responsabile della brevità della sopravvivenza.
Seguirono altre iniziative chirurgiche da parte di alcuni famosi chirurghi americani come Kantrowitz, Cooley, De Bakey, i quali eseguirono altri trapianti di cuore sull'uo-mo, ma con successi ancora inferiori a quelli di Barnard. A questo punto i ricercatori si impegnarono per risolvere questo problema. Finalmente l'obiettivo fu centrato negli anni '70 e '80 con la scoperta della ciclosporina come farmaco antirigetto.
Con l'introduzione dei farmaci antirigetto i risultati cam-biarono radicalmente e anche in Italia fu effettuato il primo trapianto cardiaco su Ilario Lazzari. Era il 14 novembre 1985 quando il chirurgo il Prof Vincenzo Gal-lucci (1935-1991) effettuò l'intervento nell’ospedale di Padova.Ilario Lazzari, visse fino al 1992, quando fu stroncato da un’infezione contratta con una trasfusione di sangue infetto.
Il secondo trapianto cardiaco quasi contemporaneamen-te (4 giorni dopo) fu eseguito a Pavia dal Professor Mario Viganò (1938).
Attualmente con le nuove tecniche chirurgiche e i pro-gressi nel campo immunologico, il trapianto cardiaco vie-ne eseguito in numerosi centri di tutto il mondo con esiti assai soddisfacenti. In riferimento all'attività chirurgica italiana, bisogna segnalare che il Prof Viganò ha inoltre eseguito il primo trapianto eterotopico di cuore (1986), il primo cuore artificiale extracorporeo (1987), il primo tra-pianto di cuore-polmone (1991), il primo trapianto-domi-no (1991); ha trapiantato il primo cuore artificiale porta-tile Novacor (1993) e il primo permanente Lion Heart (2001). In totale ha portato a termine più di 1400 tra-pianti, di cui 1050 di cuore, 50 di cuore e polmone e più di 300 tra polmone singolo e polmoni doppio. Secondo alcune statistiche sappiamo che il numero di trapianti è andato via via crescendo in tutto il mondo, passando dagli 844 trapianti eseguiti del 1985 agli oltre 5.000 nel 2015.
I dati sulle donazioni si ripercuotono in modo positivo sul numero dei trapianti; in Italia nel 2017, gli interventi totali (organi prelevati da donatore deceduto e vivente) sono stati 3921 rispetto ai 3698 del 2016 (+6%). Si tratta di una crescita consolidata che, negli ultimi 5 anni (2017-2013) registra un incremento del 27%. Aumentano i trapianti complessivi di rene (2221 nel 2017 contro i 2076 nel 2016) e di fegato (1304 rispetto ai 1220 del 2016). Sostanzialmente stabili sono i trapianti di cuore (265 nel 2017- 266 nel 2016) e di polmone (144 nel 2017-147 nel 2016).

Secondo i dati pubblicati qualche anno fa del centro A. De Gasperis di Milano la sopravvivenza a 10 anni dopo un trapianto è del 71%. Oltre l'80% dei pazienti che han-no avuto un trapianto di cuore conduce una vita norma-le. In alcune ricerche condotte nel Regno Unito il 50% dei trapiantati ritorna ad una attività lavorativa produttiva. Un esempio di elevata sopravvivenza è quella dello scrittore Ugo Riccarelli, il quale dopo aver subito un dop-pio trapianto cuore e polmoni è sopravvissuto per oltre 20 anni ed inoltre nel 2004 ha vinto il Premio Strega con "Il dolore perfetto" e nel 2013,poco dopo la sua morte,ha vinto il Premio Campiello con "L’a-more graffia il mondo".
Quali sono le criticità di questa metodica?
La più importante è la carenza di organi da trapiantare, per cui la domanda non può essere totalmente soddi-sfatta. Per questa ragione diviene assai importante, per sfruttare al meglio le risorse disponibili, bisogna selezio-nare molto bene i pazienti candidati all'intervento, ai fini di riservare il trapianto ai pazienti che possono trarne il maggiore vantaggio in termini di sopravvivenza.
In conclusioni attualmente, il trapianto cardiaco rimane il gold standard della terapia sostitutiva cardiaca ma non tutti i pazienti possono accedervi a causa della carenza di donatori, del lungo periodo di attesa nella lista trapianti e della eventuale presenza di comorbilità che rappresen- tano le controindicazioni più frequenti al trapianto.
The 2016 International Society for Heart Lung Transplan-tation listing criteria for heart transplantation: A 10-year update.
Sono stati pubblicati di recente i criteri dell'International Society for Heart Lung Transplantation del 2016 per il trapianto cardiaco. Il presidente del comitato per le linee guida Mandeep Mehra del Brigham and Women’s Hospi-tal di Boston ha dichiarato che negli ultimi 10 anni molte cose sono cambiate nella valutazione della candidatura di un paziente ad un trapianto cardiaco. Ad esempio, il supporto circolatorio meccanico con un ventricular assist device consente di valutare i pazienti che presentano quelle che, una volta, erano viste come controindicazioni relative (tumori, obesità, insufficienza renale, ipertensio-ne polmonare, etc). I pazienti con tumori trattabili posso-no trarre beneficio da un ventricular assist device, che potrebbe essere usato come presidio temporaneo in attesa che un paziente divenga un candidato idoneo al trapianto. I limiti superiori di età e peso sono stati modifi-cati ed anche alcuni pazienti selezionati di età >70 anni possono essere considerati candidati al trapianto. I pa-zienti dovrebbero perdere abbastanza peso da presen-tare un Body Mass Index (BMI) <35 prima di entrare nella lista trapianti ma, ciononostante, il paziente usual-mente aumenta significativamente di peso dopo il tra-pianto e, quindi, gli effetti collaterali come apnea not-turna, artrite, infezioni sono più frequenti nei pazienti obesi. L’inserimento nella lista trapianti, inoltre, non do-vrebbe essere basato soltanto sui punteggi relativi alla sopravvivenza e all’insufficienza cardiaca (Seattle Heart Failure Model (SHFM) e Heart Failure Score Sopravvi-venza (HFSS), dato che questi punteggi hanno delle li-mitazioni, ma si deve tener conto della fragilità del pa-ziente. La presenza di Cardiac resynchronization therapy non altera i valori attuali di cut-off di picco di VO2 al test da sforzo cardiopolmonare. Nei casi di ipertensione pol-monare trattati con LVAD, il cateterismo cardiaco destro dovrebbe essere ripetuto dopo 3-6 mesi per assicurarsi dell'eventuale reversibilità del regime pressorio polmona-re. The Journal of Heart and Lung Transplantation, Vol 35, No 1, January 2016.
Nel 2019 i trapianti sono: ne sono stati effettuati 3.813 (+2,4% rispetto al 2018). Il maggiore numero di trapianti complessivi ha riguardato:
-rene (2.137, +0,6%)
-fegato (1.302, +4,5%)
-polmone (153, +6,3%, trapianti in totale)
-cuore (245 +5,2%).
Stabili i trapianti di pancreas (42 contro i 41 dell’anno 2018).
L’utilizzo di device di assistenza ventricolare sinistra (VAD) come trattamento della fase avanzata dell'insufficienza cardiaca è notevolmente aumentato ne-gli ultimi 10 anni,vista la significativa riduzione delle complicazioni successive all’impianto come la trombosi della pompa artificiale e l’ictus che ha comportato un notevole miglioramento della sopravvivenza, specie con l’intro-duzione di modelli di nuova generazione a flusso conti-nuo (Mehra MR,et Al. N Engl J Med 2017;376:440-450).
ASSISTENZA CIRCOLATORIA MECCANICA
L' assistenza meccanica cardiaca è assai utile in tutte le situazioni di scompenso cardiaco refrattario al tratta- mento farmacologico.Tali dispositivi sono frequentemen-te utilizzati come ponte all'intervento di trapianto cardia-co. È possibile praticare l’assistenza a entrambi i ventri-coli o solo al ventricolo sinistro, quest'ultima modalità di assistenza è attualmente quella più utilizzata in conside-razione dei migliori risultati ottenuti.
Quali sono le tecniche?
1. CARDIOMIOPLASTICA.
Come supporto inotropo al ventricolo sinistro della mio-cardiopatia dilatativa, Alain Frédéric Carpentier, cardio-chirurgo di Bordeaux, per primo sperimentò la possibilità di impiegare un muscolo scheletrico (usualmente il mu-scolo grande dorsale) da avvolgere intorno al cuore e sti-molarlo con un pace-maker. Questa tecnica, gravata da una forte incidenza di eventi intraoperatori, non ha mo-strato in numerosi studi un aumento della sopravviven-za.
2. SISTEMI DI ASSISTENZA MECCANICA:
I sistemi di assistenza meccanica sono pompe elettro-meccaniche usate per il supporto circolatorio nei pazien-ti con scompenso cardiaco in fase terminale, in conse-guenza di una patologia cronica (cardiopatia ischemica, cardiomiopatia dilatativa) o in acuto (shock cardiogeno, miocardite).
Classificazione:
-a seconda che l’ assistenza supporti:
-
il ventricolo sinistro si chiama: L (left) LVAD;
-
il ventricolo destro si chiama R (right) RVAD;
-
tutte e due i ventricolari si chiama BiVAD;
-in base alle caratteristiche del flusso ematico gene-rato: pulsatile (in genere quelli di prima generazione, do-tato di escursione sisto-diastolica misurabile) o continuo (esprimibile come pressione media di perfusione in as-senza di escursione sisto-diastolica);
-in base alla durata:
I sistemi di assistenza meccanica vengono impiantati con diverse finalità terapeutiche:
.in attesa del trapianto cardiaco (Bridge To Transplan-tation, BTT);
.in alternativa altra pianto come trattamento (Destina-tion Therapy, DT), in attesa dell’eventuale recupero del-la funzione cardiaca (Bridge To Recovery, BTR);
.in attesa di decisione o di rivalutazione per trapianto (Bridge To Destination, BTD o Bridge To Candidacy, BTC).
L’indicazione di impianto di sistemi di assistenza mecca-nica come "Destination Therapy" viene considerata per quei pazienti in cui il trapianto non è indicato; d’altra parte molti pazienti con indicazione al trapianto ricevono l’impianto di un sistema di assistenza meccanica come "Bridge To Transplantation" a causa della carenza di do-natori d’organo.Tutti i sistemi di assistenza meccanica sono dotati di una via di connessione al ventricolo sini-stro chiamata “via di inflow” attraverso la quale viene prelevato il sangue proveniente dal ventricolo disfun-zionante e viene convogliato al sistema propulsivo dei si-stemi di assistenza meccanica. La via di uscita dal siste-mi di assistenza meccanica è denominata“outflow”: anch’ essa è costituita da una cannula anastomizzata chirur-gicamente all’ aorta ascendente o, in alcuni casi, discen-dente toracica.
Dai primi modelli che erano costituiti da una pompa pe-ristaltica in serie con il ventricolo sinistro, si è passati a sistemi completamente impiantabili. La seguente tabella tratta da Antonello Gavazzi mostra la classificazione dei vari supporti circolatori in base al loro posizionamento.
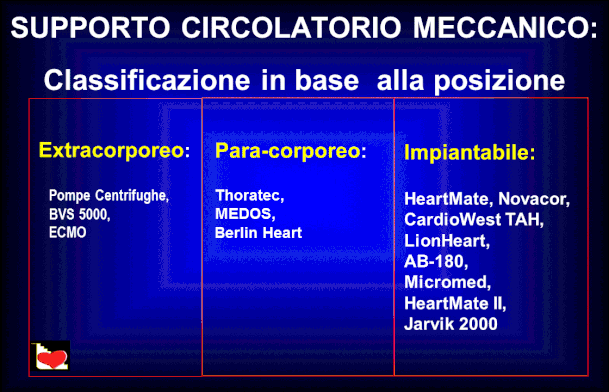
Queste tecniche possono risultare particolarmente utili nei casi in cui la disfunzione è provocata da eventi pa-tologici per i quali si ipotizza il recupero, come ad esem-pio in casi di miocardite oppure quando, per le condizioni irreversibili del danno miocardico, si è in attesa del tra-pianto. Se è presente una grave disfunzione del ventrico-lo destro l'impianto dell'assistenza meccanica limitata al ventricolo sinistro non determina significative modifica-zioni delle pressioni polmonari.
SISTEMI DI ASSISTENZA MECCANICA:
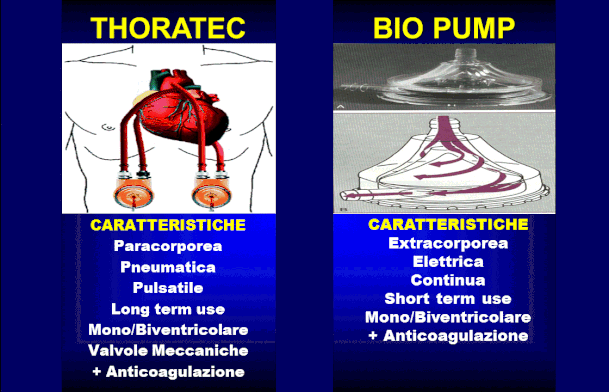
Esempi di sistemi di assistenza meccanica paracor- porei ed extracorporei:
.Pompe peristaltiche. Sono utilizzate occasionalmente, hanno la
caratteristica di non fornire un flusso pulsatile, ma continuo;
.Pompe centrifughe.Vengono utilizzate in condizioni di emergenza come
ponte al trapianto cardiaco.Esse sfrut-tano la energia cinetica prodotta dalla rapida messa in rotazione del sangue nella porzione più interna del siste-ma;
.Abiomed VAD (ventricular assistant device).E' costi- tuito da un dispositivo con due camere, camera atriale e camera ventricolare separate da una valvola di poliure-tano. Il
riempimento atriale è passivo con il sangue pro-veniente dall'atrio del paziente, mentre la camera ven-tricolare, connessa all' aorta e/o all' arteria polmonare con un tubo in Dracon,si riempie e
si svuota ritmicamen-te per mezzo di un meccanismo ad aria compressa e guidato dalla consolle di controllo;
.Thoratec/Pierce-Donachy. Il sistema comprende una
sacca in poliuretano che funziona da camera ventrico- lare e un diaframma flessibile azionato ad aria compres-sa che consente il suo svuotamento. Il sistema è inserito in un contenitore
rigido che si posiziona sulla parete ad-dominale a cui vengono collegate la cannula d'ingresso proveniente dall'atrio sinistro o dall'apice del ventricolo sinistro e la cannula di uscita
separata dal sistema da una protesi valvolare meccanica tipo Bjork-Shiley, che viene posizionata in aorta ascendente. Anche questo si-stema funge da ponte al trapianto.

Esempi di sistemi di assistenza meccanica impianta- bili:

.Thermedics Heart Mate.Il dispositivo collega l'apice del ventricolo
sinistro con l'aorta ascendente per mezzo di una cannula di Dracon.Vengono impiegati materiali che hanno una maggiore biocompatibilità rispetto al sistema Novacor, che consente una minore
intensità di terapia anticoagulante con conseguente minor rischio di emorragie. Questi sistemi di assistenza meccanica con-sentono che una percentuale più alta di pazienti venga portata al
trapianto. Heart Mate II (Thotatec Corporation, Pleasanton, CA, USA) è l’unico LVAD a flusso continuo con approvazione FDA per l’ uso sia come BTT sia come DT. Può raggiungere flussi compresi tra
3 e 10 l/min. La pompa è connessa all’ apice cardiaco con una cannula di inflow e all’ aorta con un tubo vascolare di poliestere per l’outflow e viene collocata in una tasca creata
appo-sitamente sul diaframma. Il cavo di alimentazione viene tunnellizzato attraverso la parete addominale e fatto fuo-riuscire al di sopra della spina iliaca antero-superiore destra e si
connette ad un sistema esterno costituito da un controller e dalle batterie. Secondo recenti studi, la sopravvivenza ad un anno è circa dell’80%, con un signi-ficativo miglioramento della qualità
di vita;
.Novacor. E' costituito da una pompa elettromeccanica posizionata nel
quadrante superiore sinistro dell' addome che viene messa in connessione attraverso il diaframma con due tubi in Dracon all'apice del ventricolo sinistro e all' aorta. La pompa è collegata ad una
consolle di con-trollo e ad un generatore elettrico. Per la sua semplicità e per il suo più basso ingombro, viene impiegato per l'assi-stenza circolatoria anche per tempi relativamente più
lun-ghi;
.Il dispositivo Jarvik 2000 (Jarvik Heart, Inc, New York, NY,USA) ha il
marchio CE per BTT e DT. Viene impian- tato attraverso l’apice del ventricolo sinistro e il tubo va-scolare per l’outflow è anastomizzato all’aorta ascenden- te (se
l’ approccio è sternotomico) o all’ aorta discenden- te (se è stato impiantato per via toracotomica sinistra). Esiste anche una versione pediatrica. L’ unicità di que-sto sistema consiste
nell’ impianto della pompa nella ca-mera ventricolare sinistra, senza la necessità della can-nula di inflow e della tasca per l’alloggiamento della pompa. Può fornire flussi fino a 6 l/min.
Il sistema Jarvik 2000 ha la possibilità di essere collegato al sistema di controllo non a livello addominale ma tramite un sistema “plug-in” fissato a livello della mastoide nella regione
retro-auricolare; tale ubicazione si correla con una mi-nore incidenza di infezioni del tramite del cavo. È stata riportata una significativa “durabilità” in vivo: sette anni di assistenza
continua in caso di impianto come DT;
.Heartware è una pompa centrifuga di terza generazio- ne, completamente impiantabile all’interno dello spazio pericardico, in grado di
fornire fino a 10 l/min;
.il dispositivo Incor è la prima pompa a levitazione ma-gnetica, con
flusso continuo assiale e può fornire flussi fino a 7 l/min.

3. CUORE ARTIFICIALE TOTALE
Un cuore artificiale totale impiantabile è la soluzione ideale in alternativa al trapianto cardiaco. Esso dovrebbe riprodurre totalmente un cuore umano normale con due ventricoli che mobilitano il sangue come farebbe il muscolo cardiaco, con recettori che permettono di accelerare e rallentare il cuore e cioè di aumentare il flusso o di diminuirlo a seconda delle esigenze metabo-liche dei vari organi:ad esempio quando il paziente dor-me, la frequenza cardiaca deve diminuire, quando ese-gue un esercizio fisico come il salire le scale la fre-quenza deve aumentare.
Nel tempo sono stati effettuati vari tentativi. Nel set- tembre 2010 è stato innestato un cuore artificiale per-manente nel petto di un ragazzo di 15 anni affetto da distrofia muscolare di Duchenne. Questo è stato il primo caso in cui un dispositivo è stato innestato con l'intento di mantenerlo fino al termine naturale della vita del pa-ziente: le indicazioni sono state poste perché la patologia di base non rendeva il paziente candidabile al trapianto di cuore.
Nel febbraio 2013 è stato effettuato a Siena il primo intervento della Toscana di impianto di un cuore artificiale totale. La complessa operazione è durata circa otto ore. La paziente, una 39/enne di origini lucane e residente ad Altopascio, ha mostrato di rispondere bene alle cure.
Un altro impianto è stato effettuato nel settembre 2013 su un paziente affetto da insufficienza cardiaca terminale da un’èquipe medica dell’ ospedale francese Georges Pompidou di Parigi. Il cuore artificiale è stato preparato dall’ azienda francese Carmat, dopo lunghi anni di studi e ricerche.
Nel mese di dicembre 2013 sempre a Parigi è stato trapiantato un cuore artificiale completamente autonomo ad un paziente sofferente di un’ insufficienza cardiaca terminale, con prognosi seriamente compromessa e nessuna alternativa terapeutica. I risultati a lungo termine devono essere ancora delineati.
Poiché il cuore artificiale potrebbe salvare ogni anno la vita di migliaia di pazienti senza il rischio di rigetto, assi-curando loro una qualità di vita assai vicina al normale, il successo di queste prime esperienze, fa guardare il futu-ro con maggiore ottimismo.
Nei primi di quest'anno all'Ospedale Bambino Gesù di Roma una bambina di 3 anni, affetta da miocardiopatia dilatativa, ha ricevuto un mini cuore artificiale. E' il se-condo intervento di questo tipo che viene praticato a li-vello mondiale.Un'altra operazione di questo tipo era sta-to effettuato nel 2012 condotta sempre nell'ospedale Bambino Gesù. Il mini cuore ha le dimensioni di una batteria stilo ed è stato utilizzato con successo sulla piccola paziente di 3 anni, ovviamente in attesa di un tra-pianto di cuore.
L’HeartMate 3 (HM3) è un device di assistenza ventricolare sinistra a flusso continuo di nuova gene-razione introdotto a giugno 2014,approvato in Eu-ropa nell’ottobre 2015 e sviluppato per fornire supporto circolatorio meccanico a breve termine, come bridge al trapianto cardiaco o a lungo termi-ne come terapia di destinazione,con batterie che garantiscono un funzionamento fino a circa17 h.
Le principali caratteristiche tecniche che lo con-traddistinguono sono:un rotore a levitazione com-pletamente magnetica, delle ampie vie di flusso e la generazione di un polso artificiale che insieme riducono il rischio di malfunzionamenti della pom-pa,il rischio trombotico e il traumatismo sui componenti ematici (Mehra MR,et.Al N Engl J Med 2018; 378:1386-1395).
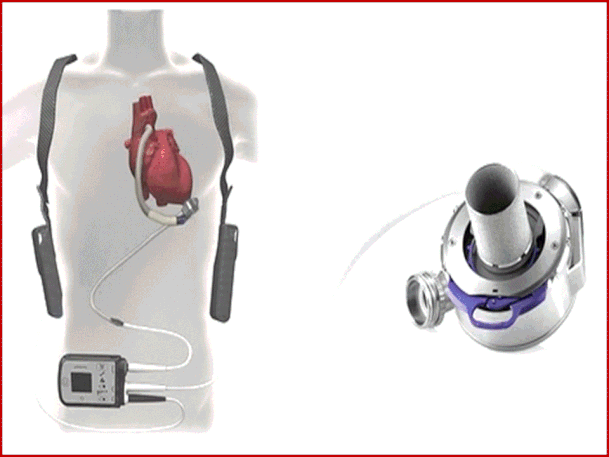
Al fine di studiare i benefici clinici di questo dispositivo è stato creato il registro prospettico,osservazionale e multi-centrico ELEVATE i cui risultati a 2 anni sono stati pubblicati sull’European Heart Journal. Dei 540 pazienti con scompenso cardiaco avanzato con ridotta funzione sistolica,osservati da marzo 2015 a febbraio 2017, 463 hanno ricevuto l’HM3 come primo impianto (coorte pri-maria) e 19 pazienti come rimpiazzo da un precedente VAD (coorte di cambio pompa). In 58 pazienti sono stati ottenuti solo dati di outcome (coorte anonima). Il 70% dei pazienti erano stati trattati precedentemente l’impianto dell’HM3 con inotropi per via endovenosa ed erano in una classe INTERMACS 1-3, il 12% dei pazienti erano in supporto circolatorio meccanico temporaneo (supporto vitale extracorporeo o VAD temporaneo) ed il 6,9% avevano un contropulsatore aortico, rappresentando quindi globalmente una coorte “real world”. Il 92% dei pazienti nella coorte primaria è stato dimesso con successo mediamente dopo un ricovero di 29 giorni di cui 7,5 in terapia intensiva. Solo il 9% ha ricevuto un trapianto cardiaco a 2 anni dall’impianto del dispositivo a causa della grande difficoltà di reperire donatori. La sopravvivenza a 24 mesi è stata del’83,4% nella coorte primaria e 74,5% nell’intero registro e l’82% dei pazienti era in classe funzionale NYHA 1 o 2 (P<0,0001). Le infezioni,la disfunzione multiorgano e l’ictus sono state le principali cause di morte (25%, 19% e 15% rispetti-vamente). Tra gli eventi avversi l’ictus si è verificato nel 10,2% (5,2% ischemici e 5% emorragici) e i sanguina-menti maggiori nel 33,3% (di cui 9,7% gastrointestinali). Un malfunzionamento del device si è osservato nel 5,4% dei pazienti ed includeva una sospetta trombosi della pompa (1,5%), disconnessioni (0,4%) o torsioni del graft di efflusso (3,5%, complicanza specifica di questo dispo-sitivo).L’impianto dell’HM3 ha determinato anche un mi-glioramento del test dei 6 minuti nei primi 6 mesi per poi arrivare ad un plateau (probabilmente a causa delle limitazioni degli attuali VAD a variare la loro velocità in ri-sposta alle attività fisiche dei pazienti) e della qualità di vita. Le limitazioni di questo registro sono sicuramente la presenza di una coorte di 58 pazienti in cui non si è po-tuto collezionare tutti i dati (coorte anonima) che potreb-bero aver avuto un impatto sull’analisi degli eventi pre-sentati. Il registro, inoltre, include un basso numero di soggetti di sesso femminile (11%), dato peraltro simile ad altri studi.Inoltre l’ELEVATE è stato monitorizzato a di-stanza e non localmente, per cui non c’è stata una ve-rifica continua delle fonti dati, sebbene si sia registrato un bassissimo tasso di abbandono a 2 anni (1%). Il regi-stro ha dimostrato i grandi passi avanti che si sono ottenuti con l’introduzione di VAD a flusso continuo ed ha ulteriormente ridotto il tasso di complicanze meccaniche (malfunzionamenti della pompa dovute a trombosi o disconnessioni del graft di efflusso) e sistemiche (ictus ed emolisi) consentendo ad un alto numero di pazienti di sopravvivere a 2 anni con una qualità di vita accettabile per la gravità della patologia di base. Sebbene il dispo-sitivo necessiti di ulteriori perfezionamenti per ridurre ad esempio i casi di torsioni del graft di efflusso, rappre-senta comunque uno strumento di particolare importan-za, se si considera la scarsità di cuori disponibili per il trapianto da donatori compatibili. Zimpfer D, et Al. Eur Heart J. 2020 Oct 14;41(39): 3801-3809.
 Cuore Sano
Cuore Sano




