COSA DOBBIAMO
ATTENDERCI
DALLA RIDUZIONE DELLA
COLESTEROLEMIA
RIGUARDO
ALLE LESIONI
ATEROSCLEROTICHE ?
Anche sull'uomo sono comparsi studi che hanno dimostrato che una aggressiva riduzione del cole-sterolo-LDL, comporta una riduzione delle lesioni aterosclerotiche.

Se prendiamo ad esempio uno studio effettuato sui vasi carotidei è stata osservata una riduzione dello spessore dell'intima-media.
Sempre sull'uomo con studi che hanno utilizzato l’ultrasonografia intravasale, dopo 18 mesi di un trattamento con farmaci ipocolesterolemizzante, è stata osservata una riduzione della progressione dell'aterosclerosi coronarica.
Uno studio di qualche anno fa ha studiato l'effetto delle statine ad alto dosaggio (Rosuvastatina 40 mg/giorno) sulle
modificazioni delle placche mediante IVUS. Sono stati studiato in particolare la regressione del volume
percentuale dell’ateroma (PAV) e il cambiamento nel vo-lume dell' ateroma.Tra novembre 2002 e ottobre 2003, sono stati arruolati 507 pazienti, che dopo essere stati sottoposti ad un esame
IVUS basalmente, hanno ricevu-to il trattamento con Rosuvastatina. Dopo 24 mesi, i pa-zienti che hanno avuto un nuovo esame IVUS valutabile sono stati 349.
Risultati:
Il livello medio della colesterolemia LDL (LDL-C) da 130,4 (34,3) mg/dL è passato a 60,8 (20,0) mg/dL,con una una riduzione media del 53,2% (P< 0,001). La cole-sterolemia ad alta densità
(HDL-C) al basale era pari a 43,1 (11,1) mg/dL e al follow-up era 49,0 (12,6) mg/dL, con un incremento del 14,7% (P<0,001). La variazione media (SD) del PAV è stata -0,98% (3,15%), con una
mediana di-0,79% (97,5% CI,-1,21% a -0,53%) p< 0,001 rispetto al basale). La variazione media (SD) del volume dell'ateroma nel sottosegmento più malato di 10 mm è stata di -6,1 (10,1) mm3, con
una mediana di -5,6 mm3 (97,5% CI, -6,8 a -4,0 mm3) (p<0.001 vs il basale). La variazione del volume totale degli ateromi ha mostrato una riduzione mediana del 6,8%; con una riduzione me-dia
(SD) di -14,7 (25,7) mm3, con una mediana di -12,5 mm3 (95% CI, da -15,1 a -10,5 mm3) (p < 0,001 vs il basale). Gli eventi avversi erano rari e simili ad altre spe-rimentazioni di
statine.
Conclusioni di questo studio:
La terapia con rosuvastatina 40 mg/giorno ha ridotto le LDL-C fino a valori medi di 60,8 mg/dL e ha aumentato HDL-C del 14,7%, con conseguente regressione signi-ficativa dell'aterosclerosi. Lo
studio ha dimostrato che Il trattamento con statine ad alto dosaggio che induce una riduzione dei livelli di LDL-C al di sotto dei livelli consi-gliati dalle guida e si accompagna a significativi
aumenti delle HDL-C,può fare regredire l'aterosclerosi nei pazien-ti affetti da malattia coronarica.

Rosuvastatin versus Atorvastatin.
Lo studio SATURN trial (Study of Coronary Atheroma by Intravascular Ultrasound: Effect of Rosuvastatin Versus Atorvastatin) ha valutato l’efficacia delle statine ad alte dosi oltre che nel ridurre gli eventi avversi cardiovasco-lari, nel rallentare la progressione dell’ aterosclerosi coro-narica attraverso la loro capacità di ridurre le lipopro-teine a bassa densità (LDL). Sono stati esaminati, dal gennaio 2008 al giugno 2009, 1.578 pazienti affetti da malattia coronarica arruolati in 208 centri e sono stati randomizzati a 2 settimane di trattamento con statine a metà del dosaggio massimo.Dopo tale periodo,1.385 pa-zienti sono stati randomizzati a ricevere una dose di di atorvastatina a 80 mg (691 pazienti) o di rosuvastatina a 40 mg (694 pazienti) e sono stati sottoposti ad una valutazione IVUS (intravascular ultrasonography) intra-coronarica. Dopo 104 settimane di trattamento 1.039 pa-zienti (75%) hanno terminato lo studio 519 pazienti nel gruppo trattato con atorvastatina e 520 pazienti trattati nel gruppo rosuvastatina);essi sono stati nuovamente sottoposti a valutazione con IVUS. I risultati hanno evi-denziato il raggiungimento di livelli molto bassi di C-LDL in entrambi i gruppi, con valori medi inferiori o uguali a 70 mg/dL che rappresenta il target delle linee guida inter-nazionali.Entrambi i trattamenti terapeutici hanno evi-denziato sorprendenti effetti sulla progressione della ma-lattia coronarica, con conseguente significativa regres-sione dell’aterosclerosi. Questi dati indicano che la ma-lattia coronarica può regredire se i livelli di colesterolo LDL e HDL sono ridotti e controllati come dimostrato in questo studio.Rispetto all’atorvastatina,la rosuvastatina ha raggiunto livelli più bassi di C-LDL (rosuvastatina 62.6 vs atorvastatina 70,2 mg/dL, differenza di -7,5 mg/dL p<0,001) e più elevati di C-HDL (rosuvastatina 48,6 vs atorvastatina 50,4 mg/dL,differenza di 1,8 mg/dL p= 0,01). La rosuvastatina, inoltre, ha mostrato un significa-tivo beneficio sulla regressione della malattia, ma la diffe-renza tra i 2 trattamenti è stata relativamente modesta mostrando che le due terapie sono simili nella loro ca-pacità di limitare la progressione o indurre la regressio-ne della malattia coronarica, anche se una differenza di efficacia non può essere esclusa sulla base delle signi-ficative differenze osservate sulla modificazione del volu-me totale dell’ateroma. Lo studio ha dimostrato che la re-gressione dell’aterosclerosi è stata osservata in circa 2/3 dei pazienti durante le 104 settimane di terapia con statine. L’end point primario (percentuale del volume dell’ ateroma) è stato raggiunto da una percentuale nume-ricamente maggiore di pazienti trattati con rosuvastatina presentando una maggiore regressione rispetto ad ator-vastatina (68,5% vs 63,2%) con una tendenza verso la significatività (p=0,07). Rosuvastatina ha ridotto dello 1,22% il volume dell’ateroma vs lo 0,99% di atorvasta-tina. Misurando invece il volume normalizzato totale dell’ ateroma,rosuvastatina ha mostrato una maggiore regres-sione (6,39 mm3 vs 4,42 mm3) statisticamente significa-tiva (p=0,02), rispetto ad atorvastatina. Inoltre la frequen-za e l’ entità della regressione è stata senza precedenti in entrambi i gruppi rispetto ai risultati di precedenti studi con valutazione IVUS. L’incidenza di effetti avversi che accompagna i benefici osservati in questo studio è stata bassa. L’aumento dei livelli degli enzimi epatici è risultata più frequente nel gruppo atorvastatina, con livelli di alani-na-amino-transferasi che erano più di 3 volte il limite su-periore del range normale in 14 pazienti, rispetto ai 5 pa-zienti nel gruppo rosuvastatina (2,0% vs 0,7%, p=0,04). I livelli di creatinchinasi superiori a 10 volte il range nor-male sono stati riscontrati in 4 pazienti trattati con ator-vastatina e in 1 paziente trattato con rosuvastatina, ma in nessuno dei due gruppi erano presenti due aumenti consecutivi dei livelli di creatinchinasi superiori a 5 volte il normale. La rabdomiolisi non è stata osservata in nessun paziente e la proteinuria non è stata significativamente differente tra i due gruppi. Nel loro insieme, i risultati indi-cano che il trattamento intensivo con statine ha portato alla regressione della malattia con pochissimi eventi av-versi. Sebbene lo studio non sia stato dimensionato per rilevare differenze tra i gruppi nei principali eventi clinici avversi, l’incidenza complessiva di infarto del miocardio è stata di 1,6% durante i 24 mesi di follow-up, e l’incidenza non differiva significativamente tra i gruppi. Il tasso di ictus è stato 0,4% e il tasso di morte per cause cardio-vascolari è stato 0,3%, senza significative differenze tra i gruppi anche in questi dati. Questo studio presenta una importante limitazione che riguarda la progressione della malattia nei pazienti trattati con placebo.Anche se questo studio comparativo non evidenzia una differenza signifi-cativa tra i gruppi di trattamento per quanto riguarda l’ end point primario, tuttavia ha dimostrato che la terapia intensiva con statine può essere somministrata in modo sicuro ed è in grado di promuovere la regressione della placca aterosclerotica in misura maggiore di quello che era stato precedentemente riportato. I risultati dello stu-dio SATURN rappresentano un fondamentale passo in avanti nello sforzo di prevenire le sequele devastanti della malattia cardiovascolare aterosclerotica attraverso l’impiego di elevati dosaggi di statine. Meeting 2011 del-l’American Heart Association, Orlando, Florida.
In conclusione vi sono evidenze che sia nell'animale da esperimento che nell'uomo, alla riduzione della coleste-rolemia, si associa un riassorbimento del materiale gras-so dalle placche lipidiche delle arterie, a cui consegue il ripristino del lume arterioso e quindi del flusso ematico.
Persistente riduzione negli eventi cardiova-scolari.
All'AHA di Chicago del 2014 sono stati presentati dal Dr. C. Packard (Università di Glasgow, Scozia) i dati del fol-low-up a 20 anni del noto trial WOSCOPS (West of Sco-tland Coronary Prevention Study); essi hanno dimostrato che il trattamento con statine per almeno 5 anni deter-mina una “persistente riduzione negli eventi cardiova-scolari” in un periodo di 2 decadi. Solo 5 anni di prava-statina possono “allungare” la vita,alterando la storia na-turale della cardiopatia abbassando i livelli del cole-sterolo LDL. Il trial di prevenzione primaria ha arruolato 6.595 uomini di età compresa tra i 45–64 anni, con elevati valori di colesterolo trattati con pravastatina, a 40 mg. Essa se assunta per 5 anni è in grado di ridurre il rischio di infarto miocardico non fatale o morte per cause cardiovascolari del 31% rispetto al placebo. Nel trial, la pravastatina ha diminuito i valori di colesterolo LDL del 26% e di colesterolo totale del 20%. A 20 anni, la mor-talità cardiovascolare si è ridotta del 27% e quella per tutte le cause del 13%.La necessità di rivascolarizza-zione coronarica era inoltre diminuita del 19% mentre l’ incidenza di scompenso cardiaco del 31%. Da segna-lare che la terapia con statine non ha dato alcun segnale di incremento di tumori in un follow-up così lungo, supportando l’idea che i vantaggi della terapia ipocole-sterolemizzante superano di gran lunga gli svantaggi. American Heart Association Scientific Session 2014.
Fra le statine naturali ricordiamo le seguenti:
•Simvastatina (nomi commerciali: Liponorm, Medipo, Sinvacor, Sivastin e Zocor);
•Lovastatina (nomi commerciali: Lovinacor, Rextat e Tavacor);
•Pravastatina (nomi commerciali: Aplactin, Prasterol, Pravaselect, Sanaprav e Selectin).
La Simvastatina viene commercializzata anche in asso-ciazione a un altro tipo di farmaco, l’Ezetimibe (nomi commerciali: Goltor, Inegy e Vytorin).
Vi sono poi altre statine, sia naturali che sintetiche, che in Italia non sono disponibili; è il caso, per esempio, di mevastatina e pitavastatina,la prima fa parte delle statine naturali, mentre la seconda rientra nel gruppo delle statine sintetiche.
Recenti evidenze hanno dimostrato che l’aggiunta ai trattamenti ipocolesterolemizzanti convenzionali di un an-ticorpo anti-PCSK97,come l'evolocumab e l'alirocumab, permette di ridurre in modo significativo la colesterolemia (fino al 60-70%) in aggiunta rispetto a quanto già fanno le statine e l'ezetimibe; questo per garantire il raggiungi-mento degli obiettivi terapeutici per le LDL-colesterolo in una larga percentuale di pazienti a ad alto rischio cardio-vascolare.
I farmaci di questa nuova classe, in Italia attualmente re-golati dall’impiego di un piano terapeutico, sono in grado di ridurre la colesterolemia inibendo la degradazione del recettore delle LDL e, quindi, favorendo la clearance delle LDL circolanti. Il buon profilo di tollerabilità di que-sta nuova classe di farmaci,associabili alle terapie ipoco-lesterolemizzanti esistenti, è stato di recente supportato dalla loro capacità di ridurre nel tempo il rischio di eventi cardiovascolari senza produrre effetti collaterali di rilievo a medio termine.
A tale proposito, l’impiego di evolocumab ed alirocumab in pazienti a rischio cardiovascolare molto alto, rispettiva-mente nei trials FOURIER e ODYSSEY OUTCOMES, ha portato ad una riduzione significativa e sovrapponibile del rischio di eventi cardiovascolari maggiori. Inoltre l’uso di alirocumab in pazienti con una recente sindrome coro-narica acuta ha consentito di ridurre anche la mortalità per tutte le cause.Nel complesso,i risultati dei trials con anticorpi anti-PCSK9 rinforzano ulteriormente il dato or-mai incontrovertibile secondo cui la riduzione della cole-sterolemia LDL ben al di sotto di 70 mg/dL in pazienti a rischio cardiovascolare molto alto produce un beneficio clinico significativo, tanto più rilevante quanto maggiore è la riduzione della colesterolemia ottenuta.
Le linee guida ESC/EAS, raccomandano di ridurre la colesterolemia LDL di almeno il 50% nei pazienti a ri-schio cardiovascolare molto alto che non ricevono un trattamento farmacologico ipolipemizzante e che hanno livelli di LDL-C compresi tra 70 mg/dL e 135 mg/dL.
Le linee guida multi-societarie americane sulla gestione della colesterolemia hanno ribadito che, in pazienti a ri-schio cardiovascolare molto alto e con LDL-C ≥70 mg/dL o non-HDL-C ≥100 mg/dL nonostante la terapia con sta-tina ed ezetimibe, l’aggiunta di un inibitore di PCSK9 è ragionevole.Anche nei paziente in prevenzione primaria con ipercolesterolemia familiare eterozigote (LDL-C non in trattamento ≥190 mg/dL), l’aggiunta di un anticorpo anti-PCSK9 può essere presa in considerazione quando l’impiego di una statina più ezetimibe non consentano di portare la colesterolemia LDL < 100 mg/dL.


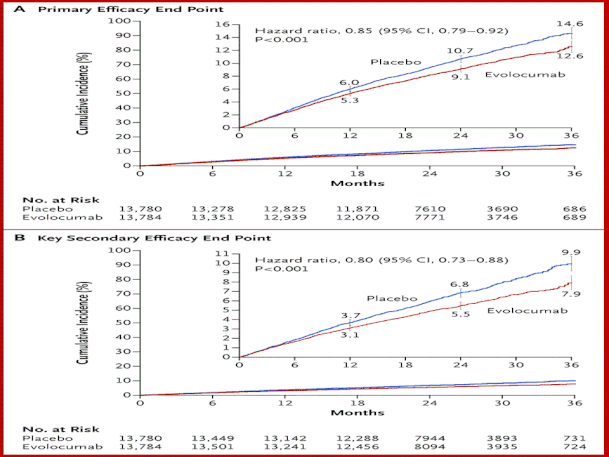
Il pannello A mostra i tassi di evento cumulativi per il end point combinato morte cardiovascolare,infarto
del mio-cardio, ictus, ospedalizzazione per angina instabile o va-scolarizzazione coronarica, e il pannello B mostra i tassi l'end point secondario morte cardiovascolare,infarto mio-cardico o
ictus. Le barre I indicano intervalli di confidenza del 95%. I tassi di Kaplan-Meier per l'obiettivo primario del gruppo evolocumab rispetto al gruppo placebo sono stati i seguenti: a 1 anno, il
5,3% (intervallo di confidenza del 95% [CI], dal 4,9 al 5,7) contro il 6,0% (95% CI, 5,6 a 6,4); a 2 anni, 9,1% (95% CI, 8,6 a 9,6) contro 10,7% (95% CI, 10,1 a 11,2); e a 3 anni, 12,6% (95% CI,
11,7 a 13,5) contro 14,6% (95% CI, 13,8 a 15,5). I tassi di Ka-plan-Meier per l'endpoint secondario nel gruppo evolo-cumab rispetto al gruppo placebo sono stati i seguenti: a 1 anno, 3,1% (95%
CI, 2,8 a 3,4) contro 3,7% (95% CI, 3,4 a 4,0); a 2 anni, 5,5% (95% CI, 5,1 a 5,9) contro 6,8% (95% CI, 6,4 a 7,3); e a 3 anni, 7,9% (95% CI, 7,2 a 8,7) contro 9,9% (95% CI, 9,2 a 10,7). I valori
P sono stati calcolati con l'uso di test di log-rank.
ODYSSEY Outcomes è il secondo studio sui risultati con un inibitore del PCSK9, che ha mostrato una ridu-zione degli endpoint LDL-C e cardiovascolari. Rispetto allo studio FOURIER, lo studio ODYSSEY Outcomes ha arruolato un gruppo di pazienti ad alto rischio, ha avuto una durata più lunga di follow-up (che va da due a cinque anni), ha coinvolto una diversa strategia di dosaggio e aveva un endpoint primario leggermente diverso.Ii risultati dello studio ODYSSEY Outcomes hanno dimostrato che il trattamento con alirocumab ha ridotto gli eventi cardiovascolari e i decessi per tutte le cause del 15% nei pazienti con sindrome coronarica acuta (ACS) e i livelli di lipoproteina aterogenica ancora alti, nonostante la terapia con dosi massime di statina. ODYSSEY Outcomes ha incluso 18.924 pazienti in 57 paesi che avevano avuto un ACS nei 12 mesi preceden-ti.La maggior parte dei pazienti (92,5%) erano arruolati a causa dei livelli di i LDL-C = 70 mg/dL. I pazienti sono stati randomizzati a iniezioni sottocutanee di alirocumab 75 mg ogni 2 settimane (n. 9.462) o placebo (n. 9.462). Il livello LDL-C da raggiungere era da 25 a 50 mg/dL.L' alirocumab è stato uptitrated a 150 mg ogni 2 settimane nei pazienti con LDL-C 50 mg/dL. I pazienti che avevano livelli di LCL-C costantemente al di sotto di 15 mg/dL sono stati commutati a placebo. Dopo un follow-up me-diano di 2,8 anni, i livelli di LDL-C erano 53,3 mg/dL nel gruppo alirocumab rispetto a 101,4 mg/dL nel gruppo placebo, con una riduzione assoluta del 54,7%. L'end-point primario dei principali eventi cardiovascolari avversi (MACE) e cioè il momento della prima comparsa di ma-lattia coronarica (CHD), l' infarto miocardico non fatale (MI),l'angina instabile che richiedeva il ricovero in ospe-dale o l'ictus ischemico è risultato significativamente più basso nel gruppo alirocumab rispetto al gruppo placebo (9,5 contro 11,1%). I ricercatori hanno osservato l'infarto del miocardio non fatale è stato ridotto del 14%, l'ictus del 27% e l'angina instabile del 39% (tutti significativi) con alirocumab rispetto al placebo. Mentre il tasso di mortalità per tutte le cause è stato significativamente inferiore del 15% con alirocumab contro placebo (3,5 vs 4,1%), non c'era alcuna differenza significativa tra i gruppi per morte da CHD (2,2 vs 2,3%) e per morte cardiovascolare (2,5 vs 2,9%). In termini di sicurezza, gli eventi avversi emergenti nel trattamento si sono verificati rispettivamente nel 75,8% e nel 77,1% dei gruppi aliro-cumab e placebo. Le reazioni minori nel sito di iniezione sono state l'unica differenza significativa tra i 2 gruppi, che si verificano nel 3,1% di coloro che ricevono alirocumab e il 2,1% di coloro che ricevono il placebo. Nell'analisi post hoc preautomatica per livello LDL-C al basale, i pazienti con un LDL-C 100 mg/dL hanno speri-mentato riduzioni in tutti gli endpoint. La riduzione del 24% della MACE si è tradotta in una riduzione assoluta del rischio (ARR) del 3,4%. La morte di CHD è stata ridotta del 28% (ARR 0,9%), la morte CV del 31%(ARR 1,3%) e la morte del 28% (ARR 1,7%). Il pannello A mostra i tassi di evento cumulativi per il end point com-binato morte cardiovascolare, infarto del miocardio, ictus, ospedalizzazione per angina instabile o vascolarizza-zione coronarica, e il pannello B mostra i tassi l'end point secondario morte cardiovascolare, infarto miocardico o ictus. Le barre I indicano intervalli di confidenza del 95%. I tassi di Kaplan-Meier per l'obiettivo primario del gruppo evolocumab rispetto al gruppo placebo sono stati i seguenti: a 1 anno, il 5,3% (intervallo di confidenza del 95% [CI], dal 4,9 al 5,7) contro il 6,0% (95% CI, 5,6 a 6,4); a 2 anni, 9,1% (95% CI, 8,6 a 9,6) contro 10,7% (95% CI, 10,1 a 11,2); e a 3 anni, 12,6% (95% CI, 11,7 a 13,5) contro 14,6% (95% CI, 13,8 a 15,5). I tassi di Kaplan-Meier per l'endpoint secondario nel gruppo evo-locumab rispetto al gruppo placebo sono stati i seguenti: a 1 anno, 3,1% (95% CI, 2,8 a 3,4) contro 3,7% (95% CI, 3,4 a 4,0);a 2 anni, 5,5% (95% CI, 5,1 a 5,9) contro 6,8% (95% CI, 6,4 a 7,3); e a 3 anni, 7,9% (95% CI, 7,2 a 8,7) contro 9,9% (95% CI, 9,2 a 10,7).I valori P sono stati cal-colati con l'uso di test di log-rank.

I pazienti sono stati randomizzati a iniezioni sottocutanee di alirocumab 75 mg ogni 2 settimane (n. 9.462) o pla-cebo (n. 9.462). Il livello LDL-C da raggiungere era da 25 a 50 mg/dL.L'alirocumab è stato uptitrated a 150 mg ogni 2 settimane nei pazienti con LDL-C 50 mg/dL. I pazienti che avevano livelli di LCL-C costantemente al di sotto di 15 mg/dL sono stati commutati a placebo.
Dopo un follow-up mediano di 2,8 anni, i livelli di LDL-C erano 53,3 mg/dL nel gruppo alirocumab rispetto a 101,4 mg/dL nel gruppo placebo,con una riduzione assoluta del 54,7%.L'endpoint primario dei principali eventi cardiova-scolari avversi (MACE) e cioè il momento della prima comparsa di malattia coronarica (CHD), l'infarto del mio-cardio non fatale (MI), l'angina instabile che richiedeva il ricovero in ospedale o l'ictus ischemico è risultato signifi-cativamente più basso nel gruppo alirocumab rispetto al gruppo placebo (9,5 contro 11,1%). I ricercatori hanno osservato l'infarto del miocardio non fatale è stato ridotto del 14%, l'ictus del 27% e l'angina instabile del 39% (tutti significativi) con alirocumab rispetto al placebo. Mentre il tasso di mortalità per tutte le cause è stato significa-tivamente inferiore del 15% con alirocumab contro place-bo (3,5 vs 4,1%), non c'era alcuna differenza significa-tiva tra i gruppi per morte da CHD (2,2 vs 2,3%) e per morte cardiovascolare (2,5 vs 2,9%). In termini di sicu-rezza, gli eventi avversi emergenti nel trattamento si so-no verificati rispettivamente nel 75,8% e nel 77,1% dei gruppi alirocumab e placebo.Le reazioni minori nel sito di iniezione sono state l'unica differenza significativa tra i 2 gruppi, che si verificano nel 3,1% di coloro che ricevono alirocumab e il 2,1% di coloro che ricevono il placebo. Nell'analisi post hoc preautomatica per livello LDL-C al basale, i pazienti con un LDL-C 100 mg/dL hanno spe-rimentato riduzioni in tutti gli endpoint. La riduzione del 24% della MACE si è tradotta in una riduzione assoluta del rischio (ARR) del 3,4%.La morte di CHD è stata ri-dotta del 28% (ARR 0,9%), la morte CV del 31% (ARR 1,3%) e la morte del 28% (ARR 1,7%).
La lomitapide è un nuovo farmaco indicato
come adiu-vante di una dieta a basso tenore di grassi e di altri far-maci ipolipemizzanti con o senza LDL aferesi in pazienti adulti affetti da ipercolesterolemia familiare omozigote. È un
inibitore della proteina di trasferimento microsomiale dei trigliceridi e, come tale, è in grado di ridurre l’assem-blaggio delle lipoproteine sia a livello epatico che
intesti-nale.

Tale attività permette a questo far-maco di consen-tire una riduzione media della coleste-rolemia LDL di circa il 40% oltre a ridurre la fre-quenza delle sedute afe-retiche.Lomitapide può causare aumenti dell’alanina ami-notransferasi, dell’ aspartato aminotran-sferasi e steatosi epatica. Lomitapide in sintesi riduce la sintesi epa-tica e intestinale delle Liporpoteine plasmatiche (VLDL e chilomicroni)agendo come inibitore selet-tivo della proteina microsomiale di trasporto dei N-trigliceridi (MTP).Il farmaco è commercializza-to in Italia con il nome di Lojuxta.


 Cuore Sano
Cuore Sano




